2026年全球自闭症研究范式转型与生物医学突破年度深度报告
at 2026.03.19 01:30 ca 自闭症科普 pv 205 by 自闭症科普网
2026年全球自闭症研究范式转型与生物医学突破年度深度报告
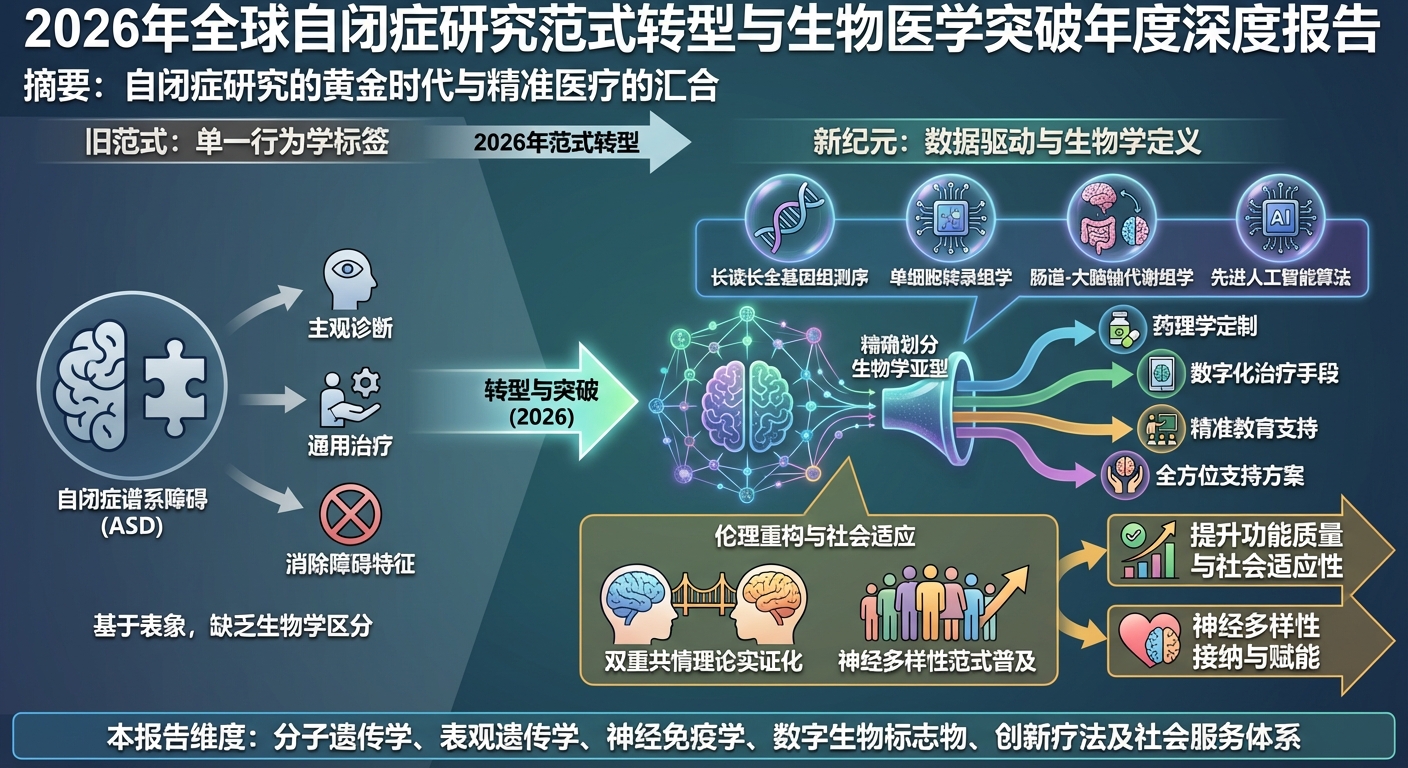
摘要:自闭症研究的黄金时代与精准医疗的汇合
自闭症谱系障碍(Autism Spectrum Disorder, ASD)的研究在2026年正式进入了一个由数据驱动、生物学定义和个体化干预为主导的新纪元。在过去的一年中,学术界不仅在揭示ASD高度异质性的底层机制方面取得了里程碑式的进展,更在诊断技术的客观化、治疗手段的数字化以及神经多样性伦理的重构上实现了跨越式发展 [1, 2, 3]。
2026年的核心科学共识在于:自闭症不再被视为一个单一的行为学标签,而是一系列具有截然不同生物学起源、发展轨迹和干预响应特征的复杂神经发育实体的集合 [1, 2, 4]。通过整合长读长全基因组测序、单细胞转录组学、肠道-大脑轴代谢组学以及先进的人工智能算法,研究者们开始能够精确地将患者划分为不同的生物学亚型,并为其量身定制从药理学到精准教育的全方位支持方案 [2, 5, 6, 7]。
此外,2026年也是学术界反思传统治疗范式的关键年份。随着“双重共情”理论的实证化和神经多样性范式的普及,研究重心已显著从“消除障碍特征”转向“提升功能质量与社会适应性” [3, 8]。本报告将从分子遗传学、表观遗传学、神经免疫学、数字生物标志物、创新疗法及社会服务体系等多个维度,系统梳理2026年自闭症领域的重大突破。
第一章 分子遗传学:从突变清单到亚型导航系统
在2026年,遗传学研究不再仅仅满足于发现新的致病基因,而是致力于解析基因变异如何通过特定的分子回路导致不同的临床表型。这一领域的突破由大规模群体队列研究和测序技术的迭代所驱动 [2, 5, 9]。
1.1 基于SPARK队列的四大生物学亚型确立
2025年下半年至2026年初,发表在《Nature Genetics》上的研究利用SPARK(目前全球最大的自闭症研究项目)中超过5,000名参与者的数据,通过机器学习模型成功识别出四种在遗传和发育轨迹上具有显著差异的亚型 [2, 4, 9]。这一发现打破了“自闭症是一个连续谱系”的传统认知,提出了“自闭症亚型”的精准分类法。
| 亚型名称 | 临床核心表型 | 共患病特征 | 遗传学倾向 | 人口比例 (SPARK样本) |
|---|---|---|---|---|
| 社交与行为挑战型 (Subtype 1) | 显著的受限与重复行为,社交沟通核心障碍 | 高发ADHD、焦虑、抑郁及情绪调节障碍 | 复杂的遗传交互作用,发育里程碑多为按时达成 | 约37% |
| 发育迟缓混合型 (Subtype 2) | 严重的早期发育里程碑延迟(语言、运动) | 较少出现内化情绪障碍(如焦虑、抑郁) | 更有可能携带高外显率的继承性变异 | 约19% |
| 中度挑战型 (Subtype 3) | 核心症状较轻,发育里程碑正常 | 心理健康状况相对良好,共患病风险最低 | 具有特定的分子通路信号特征 | 约34% |
| 广泛受累型 (Subtype 4) | 核心症状严重,伴有广泛的认知与发育障碍 | 极高风险伴随癫痫、严重焦虑及多动症状 | 新发突变 (De novo mutations) 比例显著升高 | 约10% |
[2, 4, 9]
这种分类法的意义在于,它为临床医生提供了精准的“预后地图”。例如,处于“广泛受累型”的儿童可能需要更早期的语言强化和神经调控干预,而“社交与行为挑战型”的个体则可能从针对共患ADHD或焦虑的药物治疗中获益更多 [1, 9]。研究进一步揭示,每个亚型都具有独特的生物学签名,涉及不同的神经回路和分子调节网络,这为未来的靶向药物开发奠定了基础 [2, 9]。
1.2 长读长全基因组测序(LR-WGS)攻克“缺失遗传力”
2026年3月,加州大学圣地亚哥分校(UCSD)的研究团队在自闭症遗传学领域取得了技术突破。传统的短读长测序由于无法有效覆盖复杂的基因组区域,留下了巨大的“缺失遗传力” [5]。LR-WGS技术通过一次性读取数万个碱基对,使研究者能够识别出以前隐匿的结构变异(SVs)和串联重复序列(Tandem Repeats) [5, 6]。
LR-WGS的应用带来了以下发现:
结构变异发现率提升:在对267个自闭症家庭的基因组分析中,LR-WGS发现基因破坏性结构变异的能力比传统方法高出33% [5]。
串联重复序列的深度挖掘:识别出的串联重复序列变异增加了38%,这些变异被证实直接干扰了突触蛋白的表达水平 [5]。
表观基因组集成:通过将变异数据与DNA甲基化分析相结合,研究者可以精确观察到这些突变如何改变基因的“开关状态”,而不仅仅是序列改变本身 [5, 10]。
这一技术的进步预示着,在不久的将来,通过单一的一次性遗传测试,即可解释超过50%的自闭症遗传病因,这在五年前是不可想象的 [5]。
1.3 核心致病基因与神经发育机制的新解读
2026年,学术界对某些核心基因的功能有了更深入的认识。例如,PEDS1基因被证实是干细胞转化为神经细胞过程中的关键开关,其突变会导致神经元密度和排列的异常 [11]。同时,针对MECP2基因(雷特综合征的核心致病基因)的研究也取得了突破,Huda Zoghbi博士的工作表明,MECP2突变不仅影响单基因表达,还通过调控全基因组的染色质结构来影响自闭症相关的神经可塑性 [12]。
第二章 表观遗传学与环境交互作用:风险的跨代传递
2026年的研究深刻揭示了自闭症不仅仅是静态的DNA编码问题,更是动态的基因表达调控问题。表观遗传学成为了连接遗传背景与环境暴露的关键纽带 [10, 13, 14]。
2.1 父亲高龄与精子DNA甲基化的关联
2026年1月,发表在《Aging-US》上的研究为“父亲高龄增加后代自闭症风险”提供了精细的分子机制证据 [15]。研究者发现,随着男性年龄的增长,精子中的DNA甲基化模式会发生系统性漂移,特别是在印记控制区(ICRs) [15]。
| 研究对象 | 测量工具 | 关键数据发现 | 涉及的自闭症相关基因 |
|---|---|---|---|
| 63名18-35岁健康男性 | Illumina 450K 阵列 | 14,622个与年龄相关的差异甲基化位点 (DMCs) | OTX1, PRDM16, PTPRN2, KCNQ1, DLGAP2 |
| 甲基化变化方向 | 精子发生过程 | 69%的位点表现为甲基化水平随年龄增长而下降 | GNAS, MAGEL2, GRB10 |
[15]
这些基因涉及大脑皮层发育、神经通讯和早期生长。由于精子中的这些表观遗传标记在受精后往往得以保留,它们成为了跨代风险传递的物质基础 [15]。这项研究的意义在于,它提出表观遗传学特征(而非仅仅是新发突变)是导致高龄父亲后代风险增加的主要原因,并建议建立“表观遗传钟”来评估生育风险 [15]。
2.2 创伤、压力与表观遗传“第二打击”
2026年的学术观点认为,表观遗传变异往往充当神经发育中的“第二打击”(Second Hit)。例如,父母遭受的严重创伤或环境压力可能通过DNA甲基化、组蛋白修饰和非编码RNA的变化,改变其后代的基因表达谱 [10, 13]。
这种机制解释了为何具有相同遗传背景的个体,在不同的环境压力下表现出截然不同的自闭症严重程度。研究发现,环境压力源(如饮食、毒素暴露、母体免疫激活)会通过催化DNA甲基转移酶的活性,导致突触连接相关基因的静默 [14, 16]。学术界正在探索如何通过组蛋白脱乙酰酶(HDAC)抑制剂来逆转这些不利的表观遗传改变,从而为自闭症提供新的预防或治疗路径 [10, 16]。
第三章 神经免疫学与大脑微环境:小胶质细胞的“多米诺效应”
2026年,神经炎症被公认为是自闭症病理生理学中的核心环节,而不再是次要特征。研究焦点从神经元本身转向了支撑神经元的大脑免疫环境 [11, 17, 18]。
3.1 一氧化氮信号与分子连锁反应
2026年3月7日,一项轰动学术界的研究揭示了一氧化氮(Nitric Oxide)在大脑中触发的“多米诺效应” [11, 19]。一氧化氮这种微小的信号分子,在自闭症患者脑内出现异常水平时,会引发一系列分子的链式反应,最终导致突触修剪的失败。
这种效应的生物学逻辑如下:
触发源:环境应激或遗传缺陷导致一氧化氮合酶过度激活。
分子级联:一氧化氮引发小胶质细胞的极化。
功能丧失:小胶质细胞从维护健康的“园丁”状态转变为促炎性的“破坏者”状态 [17, 18, 20]。
宏观结果:本该在发育期被剪除的多余突触被保留,导致大脑连接过度混乱,特别是前额叶皮层与边缘系统之间的超连接,这直接对应了患者的感官过敏和社交处理负荷 [21, 22]。
3.2 神经胶质细胞与突触修剪障碍
2026年的多项综述研究(如发表在《Frontiers in Psychiatry》上的文章)强调,小胶质细胞和星形胶质细胞在ASD中的作用是双重的 [17, 18, 23]。小胶质细胞通过吞噬作用精炼神经回路,而星形胶质细胞则通过调节离子稳态来维持突触传递的精准度 [17, 20]。
在自闭症大脑中,观察到的小胶质细胞密度增加实际上是一种“无效补偿”或“慢性激活”。这种慢性的炎症状态不仅损害了现有的神经连接,还产生了一系列促炎性细胞因子(如IL-6, TNF-α),这些因子通过血脑屏障进一步招募全身免疫系统的反应 [18, 21]。2026年,研究者开始利用PET成像技术实时监测自闭症患者脑内的小胶质细胞激活状态,这为抗炎疗法的介入提供了精准的时间窗口 [21, 24]。
第四章 肠道微生物组与大脑轴:精准干预的突破口
2026年,肠道-大脑轴(Gut-Brain Axis)的研究实现了从“观察相关性”到“证明因果性”的跃迁。肠道菌群不仅被视为共患胃肠道问题的根源,更被视为调控大脑认知和行为功能的“外周指挥部” [6, 25, 26, 27]。
4.1 SHIN-1:氢纳米气泡水驱动的微生态革命
2026年3月,一种名为“SHIN-1”的新型粪菌移植(FMT)疗法在临床试验中表现出色 [6]。该疗法摒弃了传统FMT所需的强力抗生素准备和肠道清洗,转而利用氢纳米气泡水制备的超低微生物浓度溶液 [6]。
这一方法的创新点及其在2026年公布的数据包括:
安全性与耐受性:由于不涉及侵入性准备,该疗法极大地减少了不良反应,特别适用于感官敏感的自闭症儿童 [6]。
核心症状的改善:在为期24周的开放标签研究中,约三分之二的参与者在社会响应量表(SRS-2)上的得分显著下降,部分患者甚至从“重度”转为“轻度”或进入“正常范围” [6]。
胃肠道无关的获益:最显著的发现是,那些没有胃肠道症状的自闭症儿童,在接受肠道菌群干预后的社交能力提升比例(45%)反而高于有胃肠道问题的儿童(24%),这彻底改变了“菌群干预仅针对腹泻/便秘”的陈旧观念 [6]。
4.2 色氨酸-犬尿氨酸(Trp-Kyn)代谢轴的深度解析
2025年6月至2026年初,由UCLA和USC合作开展的研究揭示了肠道微生物如何通过代谢物直接影响大脑功能 [26, 28]。研究发现,自闭症患儿体内产生的神经活性代谢物显著减少。
| 代谢物 | 生物学功能 | 在自闭症中的变化趋势 | 导致的行为后果 |
|---|---|---|---|
| 犬尿氨酸盐 (Kynurenate) | 神经保护,调节突触传递 | 显著水平下降 | 与严重的社交障碍和认知灵活性下降相关 [26] |
| 5-羟色胺 (Serotonin) | 情绪调节,神经元发育 | 合成路径紊乱 | 导致情绪不稳、焦虑及睡眠障碍 [28, 29] |
| 短链脂肪酸 (SCFAs) | 维持肠道屏障,调节免疫 | 多样性及含量失衡 | 引发全身性低度炎症,影响血脑屏障通透性 [27, 30] |
[26, 27, 28, 29]
基于这些发现,2026年学术界开始提倡“精准益生菌”疗法,即根据个体尿液或粪便中的代谢物谱(Metabolomic Profiling),量身定制补给菌株,如通过增加特定的乳杆菌属和双歧杆菌属来修复Trp-Kyn代谢轴 [28, 31, 32]。
第五章 数字生物标志物与AI驱动的精准诊断
2026年,诊断自闭症的方式正经历从“主观临床观察”向“客观量化测量”的范式转移。人工智能和传感器技术的发展,使得早期筛查变得前所未有的简单和准确 [33, 34, 35]。
5.1 眼动追踪与社交注意力的自动化评估
EarliPoint等FDA cleared设备的成功应用,标志着眼动追踪技术在2026年已成为临床标准。该技术通过测量幼儿在观看社交视频时,目光在面部与物体之间切换的比例,来识别自闭症早期的注意力偏差 [33, 36]。
在2026年的INSAR年会上,佐治亚理工学院的团队展示了最新的AI模型,这些模型具有以下特征:
自然交互中的自动测量:不再局限于平板电脑屏幕,通过可穿戴眼镜或环境摄像头,AI能够实时捕捉幼儿在自然玩耍过程中的“社交凝视”模式 [37]。
微细指标的捕捉:AI可以分析人眼无法观察到的眼跳幅度(Saccadic Amplitude)和眨眼率的变化,这些微细的动眼神经特征被证实是自闭症患者特有的神经信号 [35]。
高频数据采样:数据采样率高达500Hz至2000Hz,能够精准量化社会沟通障碍的严重程度,并与ADOS-2等“金标准”工具高度关联 [36, 38]。
5.2 语音声学分析与行为表型分析
除了视觉,听觉信号的AI分析在2026年也取得了突破。深度学习模型通过对婴儿哭声和幼儿非单词重复任务的音频提取,实现了高达91%的分类准确率 [33]。这些技术能够识别出人类耳朵难以察觉的韵律异常和频率抖动,为在语言能力发育之前预测自闭症风险提供了可能 [33]。
此外,数字表型(Digital Phenotyping)概念在2026年被广泛接受。通过收集电子健康档案(EHR)、睡眠监测器、运动追踪器以及家庭录像中的多模态数据,AI能够构建出一个个体的“全天候动态行为画像”,这极大地缓解了临床诊断中的“快照式评估”不足 [33, 34, 39]。
第六章 创新疗法:从虚拟现实到神经调控的临床实践
在2026年,治疗手段不再仅仅局限于ABA(应用行为分析),而是通过数字技术和神经工程实现了多元化和精准化 [40, 41, 42]。
6.1 VR 社交技能训练:Simville 与大语言模型的融合
格拉茨理工学院(TU Graz)在2026年3月展示的“Simville”系统代表了虚拟现实疗法的前沿 [41]。
技术核心:该系统集成了谷歌的Gemini 12B模型,使得虚拟环境中的社交互动不再是死板的预设对话,而是能够根据用户的语言做出具有情感色彩和即时反馈的响应 [41]。
情绪渲染:AI能够模仿人类语言中的微妙 undertone,根据对话语境展现出生气、开心或关心的情感,这对于训练患者的“社会盲视”(无法识别他人情绪)具有显著效果 [41]。
安全沙盒:由于在虚拟世界中不存在真实的社会惩罚,参与者感到更安全、更愿意尝试新的社交策略。初步研究显示,仅经过数次训练,25名参与者的社交信心即显著提升 [41]。
与此同时,Floreo VR系统也获得了FDA的重大认可。通过其沉浸式的“建立社交连接”模块,学龄儿童在12周内的交流得分显著提高,为该技术进入公立学校系统扫清了障碍 [42, 43]。
6.2 神经调控:针对特定脑环路的tDCS干预
2026年,精准神经调控试验开始针对自闭症的不同重复行为进行分型打击 [44]。
机制原理:利用高定义经颅直流电刺激(HD-tDCS),研究者试图解耦不同的大脑环路。
特定靶点:针对辅助运动区(pre-SMA)的刺激旨在减少“低级重复行为”(如身体摇晃、手部摆动);而针对左侧背外侧前额叶(dlPFC)的刺激则旨在改善“高级重复行为”(如对特定主题的过度执着、僵化的常规需求) [44]。
初步结论:2026年的中期数据表明,HD-tDCS不仅能暂时缓解重复行为,还能增强大脑的认知灵活性,为传统行为干预创造更好的神经可塑性窗口 [44]。
6.3 药物研发:GPCR 与 催产素受体的精准靶向
2026年,由欧盟资助的THERAUTISM项目宣布在分子靶点发现上取得重大进展。研究者不再泛泛地使用催产素(Oxytocin),而是识别出了特定的G蛋白偶联受体(GPCRs)作为药物靶点 [45]。
在小鼠模型中,选择性激活催产素受体(而非同时激活血管加压素受体)能够有效地恢复社交互动功能。这种“窄谱”药理学方法有望解决过去临床试验中催产素效果不稳定的难题 [45]。同时,该项目通过“Socialome”转录组数据集,开始根据小鼠的“性格档案”(如焦虑型、社交回避型)进行药物匹配,这为人类的精准药理干预提供了模型 [45]。
第七章 范式转型:精准教育与终身支持体系
2026年,学术界对自闭症的关注点正式从“童年干预”扩展到“终身跨度”。研究不仅关注如何让自闭症儿童“回归正常”,更关注如何建立一个适应神经多样性的社会体系 [1, 7, 40]。
7.1 MILE 框架:基于轨迹的精准学习模型
2026年3月提出的“医学知情的学习与教育”(Medically Informed Learning and Education, MILE)框架,标志着AI教育系统从“静态分类”向“动态发育建模”的转变 [7]。
MILE框架的核心组件包括:
纵向轨迹建模:不再根据一次考试或评估给学生贴标签,而是利用AI模型持续监测学习者的“状态依赖性变异”。
环境信号整合:将学习者的睡眠、压力、甚至当天的炎症指标(通过佩戴式设备)纳入学习分析系统,以理解行为背后的生理驱动因素 [7]。
人类辅助决策:AI不是取代老师,而是作为解释层,为教育者提供关于如何调整教学强度和环境刺激的建议,这对于“双重天才”(Twice-Exceptional)等复杂个体的支持尤为重要 [7]。
7.2 职场支持与成年期成果研究
2025年至2026年的研究开始大量关注自闭症成年人的就业成果。调查显示,工作场所的支持(如感官友好的办公环境、明确的沟通指令)比单纯的技能培训更能决定自闭症个体的职业成功 [1]。
耶鲁大学等机构提出的2026战略计划强调,服务应转向“以人为本”,重点解决影响生活质量的共患问题(如失眠、严重焦虑),而不再强制改变患者的自然社交风格,如眼神交流。这种范式的改变得到了自闭症倡导团体的广泛支持 [3, 8, 40]。
第八章 2026年INSAR年会:二十五年的回顾与未来愿景
2026年4月在布拉格举行的国际自闭症研究协会(INSAR)年会,不仅是科学成果的展示会,更是学科发展的反思会 [3, 46]。
8.1 25周年回顾:从基因猎寻到社区服务
会议的“25周年主席小组”汇聚了David Amaral, Simon Baron-Cohen等顶尖学者,讨论了领域的演变。他们一致认为,虽然基因研究取得了巨大成功,但如何将这些发现转化为社区层面的高质量医疗服务,仍是未来25年的最大挑战 [3]。
8.2 双重共情理论的科学化
Damian Milton教授在年会上的报告引起了广泛讨论。他提出的“双重共情”理论在2026年获得了更多实证支持:研究证明,非自闭症者在理解自闭症者的思维方式时同样存在困难。这一科学证据正在推动社会从“单向修复自闭症者”向“双向社会沟通建设”转变 [3]。
8.3 全球视野与资源分配
INSAR 2026强调了在低资源环境(LMIC)中的研究重要性。通过建立跨文化的诊断标准和可扩展的数字工具,研究者试图解决自闭症诊断在全球范围内的极度不均衡问题 [47, 48]。
第九章 科研生态系统:资金挑战与数据科学的崛起
2026年,自闭症研究面临着复杂的财政背景。虽然美国等国家的某些联邦资助项目(如通过DOGE计划)遭到了大幅削减,涉及金额约8000万美元,但这促使学术界转向更高效的数据共享和公私合作模式 [49]。
9.1 自闭症数据科学倡议 (ADSI)
作为对资金削减的回应,美国NIH于2025年底启动了价值5000万美元的“自闭症数据科学倡议”。该计划在2026年资助了13个项目,利用海量现有的生物库和临床数据集,专门研究基因-环境的复杂交互作用 [49]。
这种“轻资产、重数据”的研发模式正在成为主流,通过挖掘现有的15万名SPARK参与者和23andMe等商业遗传数据库,研究者得以在不进行昂贵的新招募工作的情况下,持续产生高价值的科学洞察 [2, 11]。
结论:2026年作为自闭症精准医学的分水岭
综上所述,2026年是自闭症学术研究从碎片化走向整合、从描述性转向解释性的关键一年。我们不仅在分子层面上理解了自闭症的异质性,更在技术层面上拥有了应对这种异质性的工具 [1, 2, 6]。
2026年三大核心突破点:
生物学分型的标准化:通过SPARK队列确定的四种亚型,为未来的临床试验和个体化干预提供了统一的坐标系 [2, 4]。
数字生物标志物的临床化:AI驱动的眼动追踪和行为分析不仅提高了诊断效率,更让早期干预的时间窗口提前到了出生后的第二年 [33, 35, 36]。
干预靶点的多元化:从肠道菌群的微生态调节,到针对特定脑环路的物理调控,再到融合大语言模型的虚拟现实训练,治疗手段正变得更加精准、无创且充满人文关怀 [6, 41, 44]。
尽管研究资金和伦理挑战依然存在,但2026年的进展无疑为改善全球自闭症患者及其家庭的生活质量提供了前所未有的科学基石。学术界正朝着一个不仅能“理解”自闭症,更能“支持”神经多样性共存的未来迈进 [3, 8, 40]。
免责与版权声明
每个“星星的孩子”都是独一无二的,本站分享的科普知识与干预经验仅供学习与交流,不能替代专业医疗机构的评估与诊断。
本站为公益博客,欢迎并鼓励非商业性转载与分享。转载时请注明文章出处,让我们一起传递科学与爱。